Общая химия
Отображение 353–384 из 386
-

Химия задача 68
Описание
Что называют электрическим моментом диполя? Какая из молекул HCI, НВг, HI имеет наибольший момент диполя? Почему?
Методичка здесь
1.00 $ В корзину
Методичка химия -

Химия задача 69
Описание
Какие кристаллические структуры называют ионными, атомными, молекулярными и металлическими? Кристаллы каких веществ: алмаз, хлорид натрия, диоксид углерода, цинк — имеют указанные структуры?
Методичка здесь
1.00 $ В корзину
Методичка химия -

Химия задача 7
Описание
Выразите в молях: а) 6,02 х 1022 молекул С2Н2; 6) 1,80 х 1024 атомов азота; в) 3,01 х 1023 молекул NН3. Которая мольная масса указанных веществ?
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -

Химия задача 70
Описание
Как метод валентных связей (ВС) объясняет угловое строение молекул H2S и линейное молекулы С02?
Методичка здесь
1.00 $ В корзину
Методичка химия -
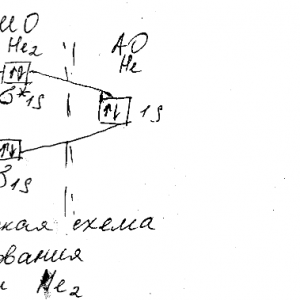
Химия задача 71
Описание
Нарисуйте энергетическую схему образования молекулы Не2 и молекулярного иона Не2 по методу молекулярных орбиталей. Как метод МО объясняет устойчивость иона Не2 и невозможность существования молекулы Не2?
Методичка здесь
1.00 $ В корзину
Методичка химия -

Химия задача 72
Описание
Какую химическую связь называют водородной? Между молекулами каких веществ она образуется? Почему М20 и HF, имея меньшую молекулярную массу, плавятся и кипят при более высоких температурах, чем их аналоги?
Методичка здесь
1.00 $ В корзину
Методичка химия -

Химия задача 73
Описание
Какую химическую связь называют ионной? Каков механизм ее образования? Какие свойства ионной связи отличают ее от ковалентной? Приведите два примера типичных ионных соединений. Напишите уравнения превращения соответствующих ионов в нейтральные атомы.
Методичка здесь
1.00 $ В корзину
Методичка химия -
Химия задача 74
Описание
Что следует понимать под степенью окисления атома? Определите степень окисления атома углерода и его валентность, обусловленную числом неспаренных электронов, в соединениях СН4, СН3ОН,НСООН, С02.
Методичка здесь
1.00 $ В корзину
Методичка химия -

Химия задача 75
Описание
Какие силы молекулярного взаимодействия называют ориентационными, индукционными и Дисперсионными? Когда возникают эти силы и какова их природа?
Методичка здесь
1.00 $ В корзину
Методичка химия -
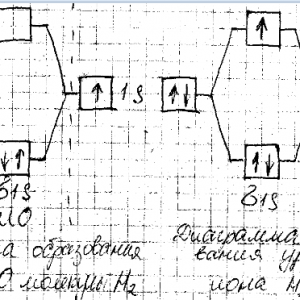
Химия задача 76
Описание
Нарисуйте энергетическую схему образования молекулярного иона Н2 и молекулы Н2 по методу молекулярных орбиталей. Где энергия связи больше? Почему?
Методичка здесь
1.00 $ В корзину
Методичка химия -
Химия задача 77
Описание
Какие электроны атома бора участвуют в образовании ковалентных связей? Как метод валентных связей (ВС), объясняет симметричную треугольную форму молекулы BF3?
Методичка здесь
1.00 $ В корзину
Методичка химия -
Химия задача 78
Описание
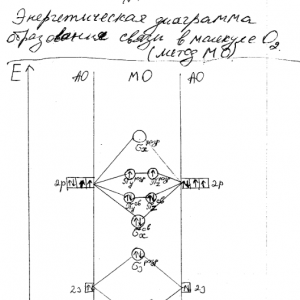
Нарисуйте энергетическую схему образования молекулы 02 по методу молекулярных орбиталей (МО). Как метод МО объясняет парамагнитные свойства молекулы кислорода?
Методичка здесь
1.00 $ В корзину
Методичка химия -
Химия задача 79
Описание
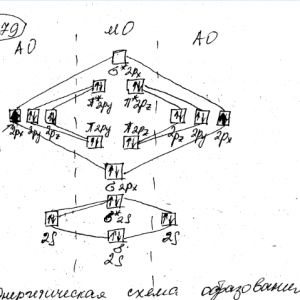
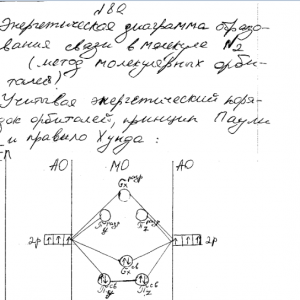
Нарисуйте энергетическую схему образования молекул F2 по методу молекулярных орбиталей (МО). Сколько электронов находится на связывающих и разрыхляющих орбиталях? Чему равен порядок связи в этой молекуле? Нарисуйте энергетическую схему образования молекулы N2 по методу молекулярных орбиталей (МО). Сколько электронов находится на связывающих и разрыхляющих орбиталях? Чему равен порядок связи в этой молекуле?
Методичка здесь
1.00 $ В корзину
Методичка химия -

Химия задача 8
Описание
Вычислите эквивалент и эквивалентную массу Н3РO4 в реакциях образования:
а) гидрофосфата; б) фосфат; в) ортофосфата.Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
Химия задача 80
Описание
Вычислите, какое количество теплоты выделится при восстановлении Fe2C>3 металлическим алюминием, если было получено 335,1 г железа.
Ответ: 2543,1 кДж.Методичка здесь
1.00 $ В корзину
Методичка химия -

Химия задача 82
Описание
Напишите выражение для константы равновесия гомогенной системы:
N2 + 3H2 ↔2NH3.
Как изменится скорость прямой реакции — образования аммиака, если увеличить концентрацию водорода в три раза?Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
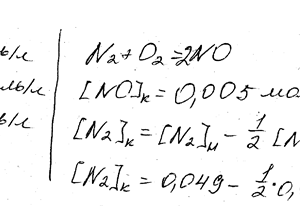
Химия задача 83
Описание
Реакция происходит по уравнению N2 + O2 = 2NO. Концентрации исходных веществ до начала реакции были: [N2] = 0,049 моль / л. Вычислите концентрацию этих веществ в момент, когда [NO] = 0,049 моль / л.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -

Химия задача 83.13
Описание
Складіть рівняння гідролізу солей. Визначте рН середовища (> 7 чи < 7). Вкажіть можливості посилення та послаблення гідролизу. CuSO4 KNO2 Методичка здесь метод 2011 химия
1.00 $ В корзину -
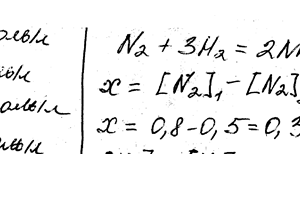
Химия задача 84
Описание
Реакция происходит по уравнению N2 + 3H2 ↔2NH3. Концентрации веществ, участвующих в ней, были: [N2] = 0,80, моль / л, [H2] = 1,5 моль / л; моль [NH3] = 0,10 моль / л. Вычислите концентрацию водорода и аммиака, когда [N2] = 0,5 моль / л.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
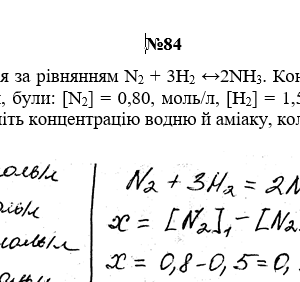
Химия задача 84.13
Описание
Реакція відбувається за рівнянням N2 + 3H2 ↔2NH3. Концентрації речовин, що беруть участь у ній, були: [N2] = 0,80, моль/л, [H2] = 1,5 моль/л; моль [NH3] = 0,10 моль/л. Обчисліть концентрацію водню й аміаку, коли [N2] = 0,5 моль/л.
Методичка здесь
1.00 $ В корзину
метод 2011 химия -
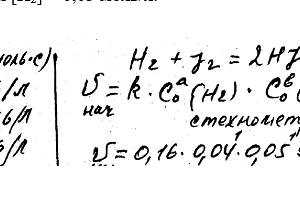
Химия задача 85
Описание
Реакция происходит по уравнению H2 + I2 = 2HI. Константа скорости этой реакции при некоторой температуре равна 0,16. Выходные концентрации реагирующих веществ [H2] = 0,04 моль / л; [I2] = 0,05 моль / л. Вычислите начальную скорость реакции и ее скорость, когда [H2] = 0,03 моль / л.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -

Химия задача 86
Описание
Рассчитайте, во сколько раз уменьшится скорость реакции, протекающей в газовой фазе, если понизить температуру от 120 до 80°С. Температурный коэффициент скорости реакции равен трем.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
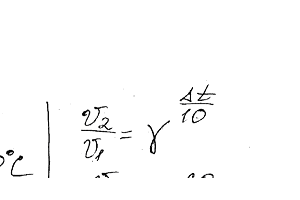
Химия задача 87
Описание
Как изменится скорость реакции, протекающей в газовой фазе при повышении температуры на 60°С, если температурный коэффициент скорости данной реакции равен двум?
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
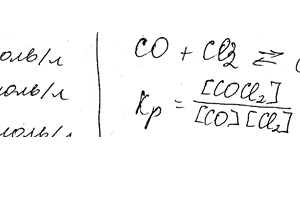
Химия задача 88
Описание
В гомогенной системе СО + Сl2 ↔ COCl2 равновесные концентрации реагирующих веществ [CO] = 0,2 моль / л; [Cl2] = 0,3 моль / л; [COCl2] = 1,2 моль / л. Вычислите константу равновесия системы и выходных концентраций хлора и СО.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
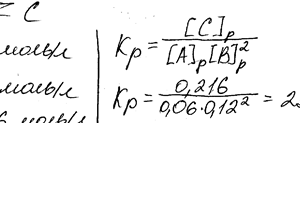
Химия задача 89
Описание
В гомогенной системе A + 2B ↔ C равновесные концентрации реагирующих газов [A] = 0,06 моль / л; [B] = 0,12 моль / л; [C] = 0,216 моль / л. Вычислите константу равновесия системы и выходных концентраций веществ А и В.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
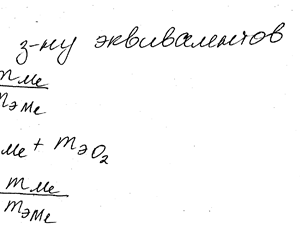
Химия задача 9
Описание
В 2,48 г оксида одновалентного металла содержится 1,84 г металла. Вычислите эквивалентные массы металла и его оксида. Чему равна мольная и атомная массы этого металла?
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
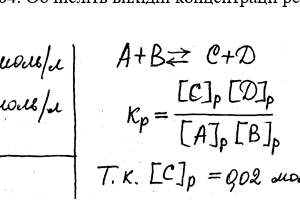
Химия задача 90
Описание
В гомогенной газовой системе A + B ↔ C + D равновесие установилась при концентрациях [B] = 0,05 моль / л и [C] = 0,02 моль / л. Константа равновесия системы равна 0,04. Вычислите исходные концентрации веществ А и В.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -

Химия задача 91
Описание
Константа скорости реакции разложения N2O, проходящей по уравнению 2N2O = 2N2 + O2, равна. Начальная концентрация N2O = 6,0 моль / л. Вычислите начальную скорость реакции и ее скорость, когда разложится 50% N2O.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
Химия задача 93
Описание
Напишите выражение для константы равновесия гетерогенной системы C + H2O (г) ↔ CO + H2. Как следует изменить концентрацию и давление, чтобы сместить равновесие в сторону обратной реакции — образование водяного пара?
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -

Химия задача 94
Описание
Равновесие гомогенной системы
4HCl (г) + O2 ↔ 2H2O (г) + 2Cl2 (г)
установилась при следующих концентрациях реагирующих веществ [H2O] p = 0,14 моль / л; [Cl2] p = 0,14 моль / л; [HCl] p = 0,20 моль / л; [O2] p = 0,32 моль / л. Вычислите исходные концентрации хлороводорода и кислорода.Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -

Химия задача 95
Описание
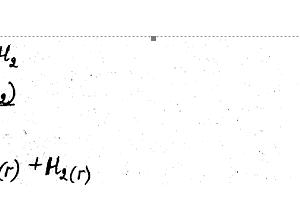
Рассчитайте константу равновесия для гомогенной системы
CO (г) + H2O (г) ↔ CO2 (г) + H2 (г)
если равновесные концентрации реагирующих веществ [CO] p = 0,004 моль / л; [H2O] p = 0,064 моль / л; [CO2] p = 0,016 моль / л; [H2] p = 0,016 моль / л. Чему равны исходные концентрации воды и CO?
Константа равновесия гомогенной системы CO (г) + H2O (г) ↔ CO2 (г) + H2 (г)
при некоторой температуре равна 1. Вычислите равновесные концентрации всех реагирующих веществ, если исходные концентрации: [CO (г)] исх. = 0,10 моль / л; [H2O (г)] исх = 0,40 моль / л.Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -

Химия задача 97
Описание
При некоторой температуре равновесие гомогенной системы 2NO + O2 ↔ 2NO2 установилась при следующих концентрациях реагирующих веществ: [NO] p = 0,2 моль / л; [O2] p = 0,1 моль / л; [NO2] p = 0,1 моль / л. Вычислите константу равновесия и исходную концентрацию NO и O2.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл