Химия
Отображение 385–406 из 406
-
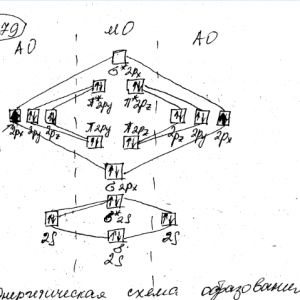
Химия задача 79
Описание
Нарисуйте энергетическую схему образования молекул F2 по методу молекулярных орбиталей (МО). Сколько электронов находится на связывающих и разрыхляющих орбиталях? Чему равен порядок связи в этой молекуле? Нарисуйте энергетическую схему образования молекулы N2 по методу молекулярных орбиталей (МО). Сколько электронов находится на связывающих и разрыхляющих орбиталях? Чему равен порядок связи в этой молекуле?
Методичка здесь
1.00 $ В корзину
Методичка химия -

Химия задача 8
Описание
Вычислите эквивалент и эквивалентную массу Н3РO4 в реакциях образования:
а) гидрофосфата; б) фосфат; в) ортофосфата.Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
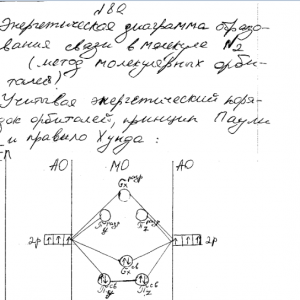
Химия задача 80
Описание
Вычислите, какое количество теплоты выделится при восстановлении Fe2C>3 металлическим алюминием, если было получено 335,1 г железа.
Ответ: 2543,1 кДж.Методичка здесь
1.00 $ В корзину
Методичка химия -

Химия задача 82
Описание
Напишите выражение для константы равновесия гомогенной системы:
N2 + 3H2 ↔2NH3.
Как изменится скорость прямой реакции — образования аммиака, если увеличить концентрацию водорода в три раза?Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
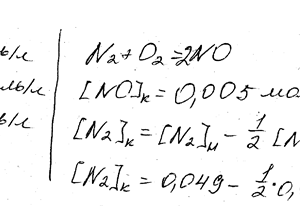
Химия задача 83
Описание
Реакция происходит по уравнению N2 + O2 = 2NO. Концентрации исходных веществ до начала реакции были: [N2] = 0,049 моль / л. Вычислите концентрацию этих веществ в момент, когда [NO] = 0,049 моль / л.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -

Химия задача 83.13
Описание
Складіть рівняння гідролізу солей. Визначте рН середовища (> 7 чи < 7). Вкажіть можливості посилення та послаблення гідролизу. CuSO4 KNO2 Методичка здесь метод 2011 химия
1.00 $ В корзину -
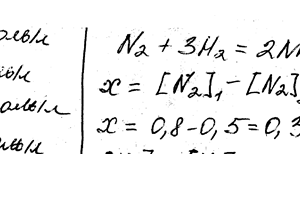
Химия задача 84
Описание
Реакция происходит по уравнению N2 + 3H2 ↔2NH3. Концентрации веществ, участвующих в ней, были: [N2] = 0,80, моль / л, [H2] = 1,5 моль / л; моль [NH3] = 0,10 моль / л. Вычислите концентрацию водорода и аммиака, когда [N2] = 0,5 моль / л.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
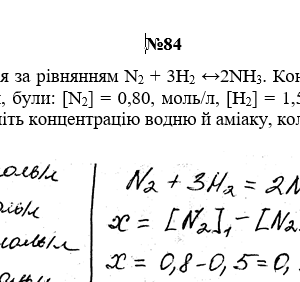
Химия задача 84.13
Описание
Реакція відбувається за рівнянням N2 + 3H2 ↔2NH3. Концентрації речовин, що беруть участь у ній, були: [N2] = 0,80, моль/л, [H2] = 1,5 моль/л; моль [NH3] = 0,10 моль/л. Обчисліть концентрацію водню й аміаку, коли [N2] = 0,5 моль/л.
Методичка здесь
1.00 $ В корзину
метод 2011 химия -
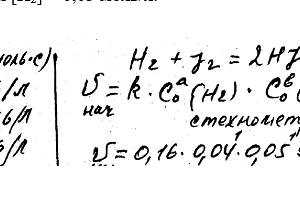
Химия задача 85
Описание
Реакция происходит по уравнению H2 + I2 = 2HI. Константа скорости этой реакции при некоторой температуре равна 0,16. Выходные концентрации реагирующих веществ [H2] = 0,04 моль / л; [I2] = 0,05 моль / л. Вычислите начальную скорость реакции и ее скорость, когда [H2] = 0,03 моль / л.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -

Химия задача 86
Описание
Рассчитайте, во сколько раз уменьшится скорость реакции, протекающей в газовой фазе, если понизить температуру от 120 до 80°С. Температурный коэффициент скорости реакции равен трем.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
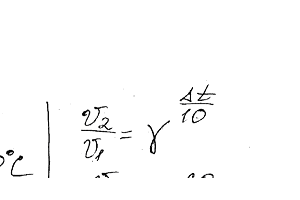
Химия задача 87
Описание
Как изменится скорость реакции, протекающей в газовой фазе при повышении температуры на 60°С, если температурный коэффициент скорости данной реакции равен двум?
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
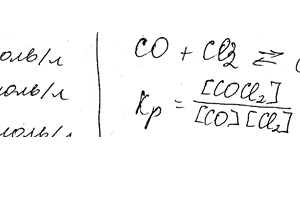
Химия задача 88
Описание
В гомогенной системе СО + Сl2 ↔ COCl2 равновесные концентрации реагирующих веществ [CO] = 0,2 моль / л; [Cl2] = 0,3 моль / л; [COCl2] = 1,2 моль / л. Вычислите константу равновесия системы и выходных концентраций хлора и СО.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
Химия задача 89
Описание
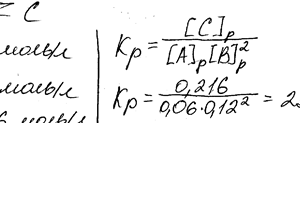
В гомогенной системе A + 2B ↔ C равновесные концентрации реагирующих газов [A] = 0,06 моль / л; [B] = 0,12 моль / л; [C] = 0,216 моль / л. Вычислите константу равновесия системы и выходных концентраций веществ А и В.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
Химия задача 9
Описание
В 2,48 г оксида одновалентного металла содержится 1,84 г металла. Вычислите эквивалентные массы металла и его оксида. Чему равна мольная и атомная массы этого металла?
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
Химия задача 90
Описание
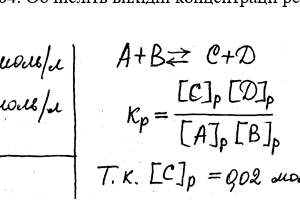
В гомогенной газовой системе A + B ↔ C + D равновесие установилась при концентрациях [B] = 0,05 моль / л и [C] = 0,02 моль / л. Константа равновесия системы равна 0,04. Вычислите исходные концентрации веществ А и В.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -

Химия задача 91
Описание
Константа скорости реакции разложения N2O, проходящей по уравнению 2N2O = 2N2 + O2, равна. Начальная концентрация N2O = 6,0 моль / л. Вычислите начальную скорость реакции и ее скорость, когда разложится 50% N2O.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
Химия задача 93
Описание
Напишите выражение для константы равновесия гетерогенной системы C + H2O (г) ↔ CO + H2. Как следует изменить концентрацию и давление, чтобы сместить равновесие в сторону обратной реакции — образование водяного пара?
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -

Химия задача 94
Описание
Равновесие гомогенной системы
4HCl (г) + O2 ↔ 2H2O (г) + 2Cl2 (г)
установилась при следующих концентрациях реагирующих веществ [H2O] p = 0,14 моль / л; [Cl2] p = 0,14 моль / л; [HCl] p = 0,20 моль / л; [O2] p = 0,32 моль / л. Вычислите исходные концентрации хлороводорода и кислорода.Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -

Химия задача 95
Описание
Рассчитайте константу равновесия для гомогенной системы
CO (г) + H2O (г) ↔ CO2 (г) + H2 (г)
если равновесные концентрации реагирующих веществ [CO] p = 0,004 моль / л; [H2O] p = 0,064 моль / л; [CO2] p = 0,016 моль / л; [H2] p = 0,016 моль / л. Чему равны исходные концентрации воды и CO?
Константа равновесия гомогенной системы CO (г) + H2O (г) ↔ CO2 (г) + H2 (г)
при некоторой температуре равна 1. Вычислите равновесные концентрации всех реагирующих веществ, если исходные концентрации: [CO (г)] исх. = 0,10 моль / л; [H2O (г)] исх = 0,40 моль / л.Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -

Химия задача 97
Описание
При некоторой температуре равновесие гомогенной системы 2NO + O2 ↔ 2NO2 установилась при следующих концентрациях реагирующих веществ: [NO] p = 0,2 моль / л; [O2] p = 0,1 моль / л; [NO2] p = 0,1 моль / л. Вычислите константу равновесия и исходную концентрацию NO и O2.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
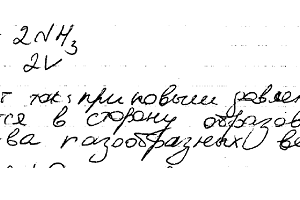
Химия задача 98
Описание
Почему при изменении давления смещается равновесие системы N2 + 3H2 ↔2NH3 и не смещается равновесие системы N2 + O2 = 2NO? Ответ обоснуйте на основе расчета скорости прямой и обратной реакции в этих системах до и после изменения давления. Напишите выражение для констант равновесия каждой из данных систем.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл -
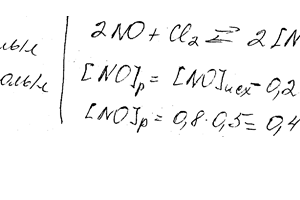
Химия задача 99
Описание
Исходные концентрации [NO] исх и [Cl2] исх в гомогенной системе 2NO + Cl2 ↔ 2NOCl составляют соответственно 0,5 и 0,2 моль / л. Вычислите константу равновесия, если к моменту наступления равновесия прореагировало 20% NO.
Методичка здесь
1.00 $ В корзину
методичка химия 2013
Методичка на украинском языке
метод усл